【】抗悪性腫瘍薬、血管新生阻害薬、受容体型チロシンキナーゼ阻害薬
用法・用量
犬:
PatnaikグレードII(中間型)またはIII(未分化型) の再発した皮膚の肥満細胞腫:[添付文書]
3.25 mg/kg PO q2day
※状態により適宜減量 (0.5mg/kgごとの減量とし、最低用量は2.20mg/kgと する)または休薬(2週間まで)を行う。投与開始6週間は毎週、その後は6週おきに再診。
乳腺腫瘍:[1]
神経内分泌腫瘍:[2]
GIST消化管間質腫瘍:[2]
肛門嚢腺癌:[2]
2.5 mg/kg PO 毎週月、水、金 8週間以上 [8]
2.75 mg/kg PO q48h、または、月、水、金 [9]
インスリノーマ:[3]
皮膚組織球腫 complex:[VMN][4]
甲状腺癌:
内分泌腫瘍:
肺腫瘍:
手術単独:145日、手術+トセラニブ:191日 [10]
猫:
口腔内扁平上皮癌:[5][6]
※NSAIDsとの併用(メロキシカム[7])
各種癌:[7]
※メロキシカム併用。鼻腔腺癌、乳腺癌、皮膚癌など、ただし症例数少ない
うさぎ:
フェレット:
ハリネズミ:
齧歯類:
鳥類:
爬虫類:
参考事項
禁忌:
注意事項:
副作用:
食欲不振、下痢、消化管出血、貧血、低アルブミン血症、好中球減少症、肝毒性、腎毒性
相互作用:
その他:
参考資料
1. PDGFR-α, PDGFR-β, VEGFR-2 and CD117 expression in canine mammary tumours and evaluation of the in vitro effects of toceranib phosphate in neoplastic mammary cell lines
2. The role of toceranib phosphate in dogs with non-mast cell neoplasia: A systematic review
3. Toceranib phosphate in the management of canine insulinoma: A retrospective multicentre study of 30 cases (2009-2019)
4. Histiocytic Diseases
5. Retrospective evaluation of toceranib phosphate (Palladia) in cats with oral squamous cell carcinoma
6. Tolerability of toceranib phosphate (Palladia) when used in conjunction with other therapies in 35 cats with feline oral squamous cell carcinoma: 2009-2013
7. Low dose meloxicam is safe and tolerable when combined with toceranib phosphate in cancer-bearing cats
8. Response and outcome following toceranib phosphate treatment for stage four anal sac apocrine gland adenocarcinoma in dogs: 15 cases (2013-2017)
9. Evaluation of toceranib for treatment of apocrine gland anal sac adenocarcinoma in dogs
10.Assessment of postoperative adjuvant treatment using toceranib phosphate against adenocarcinoma in dogs
[薬剤添付文書]
- 【動】パラディア錠®︎ [動物用医薬品等データベース]
[参考文献等]

- 心疾患を診る際にやっておくべきこと!知っておくべきこと! 堀 泰智先生の「循環器シリーズ」 第4回 液体貯留の鑑別と治療~堀が気を付けている事~ vol.06
- 2020 JFVSS オンライン夏祭り 4. 悪性腫瘍における分子標的薬の使い分け イマチニブ vs. トセラニブ
- 瀬戸口 明日香先生の「明日から役立つ」シリーズ 第19回 臨床腫瘍学 総論2:化学療法 Part 2 vol.08
- やっぱり そーだったんだ! I knew it! 知っていたけど 聞いて納得シリーズ第6回 腫瘍内科学セミナー 獣医腫瘍学における最近の躍進:トップ10(横浜) vol.09
- やっぱり そーだったんだ! I knew it! 知っていたけど 聞いて納得シリーズ第6回 腫瘍内科学セミナー 獣医腫瘍学における最近の躍進:トップ10(三重) vol.08
- VMN-JFVSSチャリティーレクチャー 犬と猫のあるある 2017 腫瘍性疾患のあるある vol.01
- 瀬戸口 明日香先生の「明日から役立つ」シリーズ 第11回 犬の肥満細胞腫 vol.07
- VMNスペシャルセミナー2015 腫瘍内科学スペシャルセミナー 「今だから聞ける 過去から現在までの腫瘍治療データの全て!」 肥満細胞腫瘍:最新で最大の知見 vol.13
- <みんなの疑問解消編>腫瘍科 Vol.11
- <みんなの疑問解消編>外科(軟部外科、腫瘍外科) Vol.9

<1> 測定可能な犬の肥満細胞腫瘍に対する少分割放射線療法とトセラニブ、プレドニゾロン療法についての多施設前向き試験
<2> 悪性腫瘍に罹患した犬における低用量シクロフォスファミドと組み合わせたトセラニブの臨床的そして免疫調節効果
<3> 犬のがんにおけるリン酸トセラニブ療法に対する反応を評価するための連続 18FDG-PET/CTの予備的評価
<4> 犬における切除不能な肥満細胞腫の治療のためにパルス投与したリン酸トラセニブとロムスチン
<5> 犬の収縮期血圧と蛋白尿に対するリン酸トセラニブの影響
<6> 犬のステージ4の肛門嚢アポクリン腺癌に対するリン酸トセラニブ投与後の反応および転帰:15例(2013~2017年)
<7> 固形腫瘍に罹患し、リン酸トセラニブで治療した犬における造影CTによる腫瘍増強の評価
<8> プレドニゾンとトセラニブまたはビンブラスチンで治療した犬の肥満細胞腫における奏効予測因子としてのc-kit変異と局在状態
<9> 猫の転移性乳癌:異なる治療モダリティにおける予後因子、転帰、および比較――後ろ向き多施設研究
<10> 犬の測定可能な癌腫に対する治療に対する1日3 Gy × 10日間の緩和的3D原体照射放射線治療プロトコールにトセラニブを合わせた治療法の忍容性を評価する予備的研究
<11> 犬の肛門腺アポクリン腺癌における免疫組織化学を利用したPDGFR-βの発現およびキット
<12> 担癌犬(肥満細胞腫を除く)に対するリン酸トセラニブ(パラディア(Palladia®))およびピロキシカム併用治療における安全性の評価: フェーズⅠ(用量設定)試験
<13> 担癌犬(肥満細胞腫瘍を除く)に対するリン酸トセラニブ(Palladia®)およびピロキシカムの組み合わせの安全性評価: フェーズI用量設定試験
<14> 固形腫瘍(*)に対するリン酸トセラニブ(Palladia®)の生物学的活性に関する予備的確証
<15> カルボプラチンまたはトセラニブを併用してピロキシカムで治療した犬3頭における原発性前頭洞扁平上皮癌
<16> 犬の切除不能または再発性の肥満細胞腫に対するトセラニブとロムスチンの併用治療において高い頻度で発生した強い毒性について: ヨーロッパにおける多施設研究
<17> 犬の切除不能または再発性の肥満細胞腫に対するトセラニブとロムスチンの併用治療において高い頻度で発生した強い毒性について: ヨーロッパにおける多施設研究
<18> リン酸トセラニブによる猫の胃間質細胞腫瘍(GIST)の治療: 症例研究
<19> 転移性腎細胞癌に罹患したダックスフンドにおいて生存期間の延長が認められた1例
<20> 犬におけるインスリノーマの管理に用いるトセラニブリン酸塩について: 30例に関する回顧的多施設研究(2009~2019)
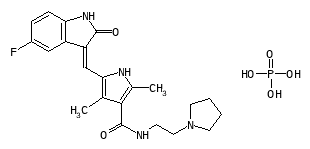
[WR2307,VQ2307:トセラニブ]
コメント